COVID-19 Diagnostics Market Size, Share & Impact Analysis, By Product (Instruments and Reagents & Kits), By Technology (Polymerase Chain Reaction [PCR], Enzyme-Linked Immunosorbent Assay [ELISA], Lateral Flow Immunoassay [LFIA], and Others), By Sample Type (Oropharyngeal & Nasopharyngeal Swabs, Nasal Swabs, Blood, and Others), Durch Setzen (Laborbasiert und Point of Care), nach Endbenutzer (Krankenhäuser & Kliniken, Laboratorien & Diagnosezentren, Heimtests und andere) und regionale Prognose, 2022-2029
WICHTIGE MARKTEINBLICKE
Der Bericht enthält zwei Szenarien für den globalen COVID-19-Diagnostikmarkt.
Szenario 1: Dieses Szenario betrachtet eine „endemische“ Situation, in der die Covid-19-Pandemie im Prognosezeitraum voraussichtlich ein endemisches Stadium erreichen wird.
Szenario 2: In diesem Szenario wird der Markt ein „zyklisches Wachstum“ beobachten, wenn man zukünftige Wellen mit anderen Varianten und die Auswirkungen von Faktoren wie Impfung und Herdenimmunität berücksichtigt.
Die globale Marktgröße für Covid-19-Diagnostik im Wert von 46,76 Milliarden USD im Jahr 2021. Für diesen Markt haben wir zwei Szenarien in Betracht gezogen. Gemäß dem ersten Szenario wird die Marktgröße voraussichtlich von 23,79 Milliarden USD im Jahr 2022 auf 8,91 Mrd. USD bis 2029 fallen, was während des Prognosezeitraums einen CAGR von -13,1% aufweist. Nordamerika dominierte den COVID-19-Diagnostikmarkt mit einem Marktanteil von 26,73% im Jahr 2021. Im Januar 2020, der den Coronavirus-Ausbruch für einen Notfall für öffentliche Gesundheit erklärte. Der plötzliche exponentielle Anstieg der Anzahl der COVID-19-Fälle führte dazu, dass die Diagnostik für Covid-19 aufgetreten ist. Die zunehmende Anzahl von Fällen hat das Marktwachstum vorantreiben.
Gemäß dem zweiten Szenario wird die Marktgröße voraussichtlich von 48,64 Milliarden USD im Jahr 2022 auf 39,68 Mrd. USD bis 2029 fallen, was während des Prognosezeitraums einen CAGR von -2,9% aufweist. Das globale Marktwachstum ist auf den plötzlichen Anstieg der Zahl der Covid-19-Fälle zurückzuführen, da neue Covid-19-Wellen auftreten.
Covid-19-Auswirkungen
Der Covid-19-Ausbruch führte zur Entstehung der COVID-19-Diagnostik
Das plötzliche Auftreten der Covid-19-Krise hat zu einem Anstieg der Diagnostikaktivitäten, der Behandlungsverfahren und der Anstieg der F & E-Aktivitäten zur Entwicklung von Diagnostika wie molekularen Tests und Pflegetests verursacht. Die wachsende Nachfrage nach COVID-19-Diagnostikverfahren und -produkten hat in der Gesundheitsbranche immense Chancen geschaffen, die den Markt erhöht. Diagnostische Unternehmen wie Thermo Fisher Scientific, Abbott, Roche und Bio-Rad haben verschiedene Technologien entwickelt, um die Erkennung und Behandlung gegen Covid-19-Infektionen zu verbessern. Im April 2020 listete er zwei COVID-19-Diagnose-Tests auf, Echtzeit-PCR-Coronavirus (Covid-19) und Cobas SARS-CoV-2 Qualitativer Assay; Beide Tests sindIn-vitro-Diagnostik.
Angesichts der zunehmenden Anzahl von COVID-19-Fällen, dem mangelnden Vorhandensein von therapeutischen oder Impfstoffen und dem Anstieg der staatlichen Fokus auf die Verhinderung einer weiteren Ausbreitung von Covid-19 wurde eine erhöhte Nachfrage nach zeitlich effizienten Tests beobachtet. Die Hauptakteure auf dem Markt haben ihren Fokus auf die Entwicklung zeitlicher und genauer Testkits erhöht. Zum Beispiel hat die US-amerikanische Food and Drug Administration (FDA) eine Notfallverwalterin (EUA) an Sofia 2 SARS Antigen FIA zum Nachweis von SARS-CoV-2 in Nasopharyngeal- und Nasenabstrich-Proben herausgegeben. Anschließend haben viele Unternehmen die COVID-19-Diagnostik-Kits eingeführt. In Dezember 2021 wurde eine weitere Instanz hervorgehoben. Seit der Pandemie hat die US-amerikanische FDA über 350 Diagnostiktests für Covid-19 zugelassen, darunter 235 Molekular-, 34-Antigen- und 88-Antikörper-basierte Tests.
Darüber hinaus konzentrierten sich die Marktteilnehmer auf die Einführung technologischer Fortschritte, um effiziente diagnostische Produkte und Dienstleistungen bereitzustellen. Im November 2021 kündigte Siemens HealthCare GmbH im November 2021 die Entwicklung des Schweregorithmus von Atellica Covid-19 an, der dazu beiträgt, das potenzielle Fortschreiten von Krankheiten und lebensbedrohlichen Multi-Organ-Dysfunktion bei CoVID-19-Patienten vorherzusagen.
Die plötzlichen Ausbrüche neuer Covid-19-Stämme und die zunehmende Nachfrage nach genauen diagnostischen Eingriffen sollen dem globalen Markt an Dynamik verleihen. Covid-19-Beschränkungen hatten jedoch einen geringfügigen Einfluss auf die Lieferkette.
Neueste Trends
Point of Care -Tests, um aufgrund der frühen Diagnose, des verbesserten Zugangs und einer schnelleren Turnaround -Zeit eine Traktion zu erlangen
RT-PCR wurde aufgrund ihrer hohen Genauigkeit als Standardtest für die COVID-19-Diagnose angesehen, es kann jedoch etwa 24 Stunden dauern, bis die Ergebnisse erzielt werden. Manchmal ist jedoch dringende Tests erforderlich. Point of Care/Rapid Covid-19-Diagnostikstests haben eine wichtige Rolle bei der Kontrolle der Ausbreitung der Krankheit und der Erleichterung der Aufhebung verschiedener Einschränkungen durch eine erhöhte Anzahl täglicher Tests gespielt.
In-vitro-diagnostische Unternehmen und Regierungen haben sich auf die Entwicklung zuverlässigerer Tests konzentriert und schnellere Ergebnisse zu erheblich geringeren Kosten liefern. Bis Juli 2021 mehr als 500 Covid-19POC -DiagnoseTests waren auf dem Markt erhältlich.
Im Oktober 2021 investierte das Department of Health and Human Services (HHS) mehr als 560 Mio. USD, um die Entwicklung und Herstellung von CoVID-19-Tests, einschließlich schneller Diagnoseprodukte, zu unterstützen.
Die zunehmende Nachfrage nach zeitlichem und genauen Tests und steigenden F & E-Investitionen durch In-vitro-Diagnostik-Unternehmen sind die wichtigsten Trends, die das Marktwachstum steigern werden.
Antriebsfaktoren
Steigende Prävalenz von Coronavirus -Erkrankungen, um den Nachfrage nach diagnostischen Geräten und Kits zu befeuern
Der plötzliche Anstieg der infektiösen Coronavirus-Erkrankung, die zu einer globalen Pandemie führte, führte zu einer eskalierenden Nachfrage nach diagnostischen Verfahren und Produkten für Covid-19. Laut Worldometer -Statistik hat es weltweit zu einem kontinuierlichen Anstieg der täglichen täglichen Fälle gekommen. Nach Angaben der Weltgesundheitsorganisation (WHO) waren ab dem 18. Mai 2021 163,3 Millionen Menschen weltweit mit Covid-19 betroffen. Der kontinuierliche tägliche Anstieg der Fälle hat die Einführung diagnostischer Tests zur frühen Behandlung für Patienten gestiegen. Sogar die aufstrebenden Volkswirtschaften wie Brasilien hatten einen bemerkenswerten Anstieg der Anzahl der Fälle und lag bis Mai 2021 bei 15,9 Millionen.
Diese Faktoren erhöhen wahrscheinlich den Umsatz von Reagenzien und Kits, die zur Erkennung von Coronavirus -Infektionen verwendet werden. Darüber hinaus dürften steigende F & E -Aktivitäten das Marktwachstum während des Prognosezeitraums vorantreiben. Mehrere Unternehmen tätigen höhere Investitionen, um die Entwicklung diagnostischer Lösungen zu unterstützen. Zum Beispiel investierten die National Institutes of Health (NIH) im Juli 2020 248,7 Mio. USD in neue Technologien, um Herausforderungen im Zusammenhang mit der COVID-19-Diagnostik (die SARS-CoV-2 Coronavirus erkennt).
Einführung innovativer Produkte, um das Marktwachstum voranzutreiben
Der Schutz des Menschenlebens ist das wichtigste Element des Gesundheitssystems während einer pandemischen Situation. Die steigende Nachfrage nach zeitlichem und effektiven Tests hat Pharmazeutikum geführt undMedizinproduktUnternehmen, die in F & E investieren, um neuartige Testkits und Assays zu starten. Große und kleine Unternehmen sowie Startups führen Produkte für Patienten und das Gesundheitswesen ein. Beispielsweise kündigte eine genaue Diagnose im April 2020 die Einführung eines Antikörpertests zur Diagnose von Covid-19 an. Dieser serologische Test wird durchgeführt, indem Speichelproben gesammelt und analysiert werden, um das Coronavirus -Antigen nachzuweisen. In einem anderen Fall kündigte CSOVIS im Mai 2021 den Start des COVID-19-Rapid-Antikörper-Tests an, mit dem IgG- und IgM-Antikörper getestet werden können. Ab Januar 2022 wurden von den Regulierungsbehörden in Nordamerika, Europa und im asiatisch -pazifischen Raum rund 700 Tests verfügbar oder genehmigt.
Die Anzahl der zugelassenen Produkte für einige der großen Unternehmen ist wie folgt:
- Abbott - 13 Tests genehmigt/verfügbar
- Quidel - 8 Tests genehmigt/verfügbar
- Roche - 7 Tests genehmigt/verfügbar
Daher wirkt sich das Vorhandensein einer unterschiedlichen Anzahl von diagnostischen Produkten für Covid-19 und die Steigerung der Investitionen nach den wichtigsten Marktteilnehmern auf den globalen Markt positiv aus.
Rückhaltefaktoren
Strenger regulatorischer Rahmen zur Entwicklung neuer Testkits zur Begrenzung des Marktwachstums
Dieser Markt hat zwar enormes Potenzial und bevorstehende Möglichkeiten. Einige Herausforderungen dürften das Wachstum des globalen Marktes behindern. Aufgrund des kontinuierlichen Anstiegs der Covid-19-Infektionen weltweit hat die Nachfrage nach besseren, sichereren und schnelleren Erkennungskits, um Patienten eine erfolgreiche Behandlung zu bieten, Chaos auf dem Diagnostikmarkt geschaffen. Hersteller müssen jedoch strenge regulatorische Einschränkungen durchlaufen, um neuartige Kits zu starten, obwohl diese diagnostischen Tools dringend benötigt werden. Zum Beispiel hat jedes Land seine Aufsichtsbehörde in unterschiedliche Vorschriften und Richtlinien für Hersteller umzusetzen. Um die Sicherheit von Produkten zu gewährleisten, haben die US -amerikanische Food and Drug Administration (FDA), die Zentren für die Kontrolle und Prävention von Krankheiten (CDC) und andere Aufsichtsbehörden ihre Richtlinien aktualisiert. Darüber hinaus dürften steigende Haushaltsbeschränkungen im Prognosezeitraum auch das Covid-19-Diagnostikwachstum auswirken.
SEGMENTIERUNG
Durch Produktanalyse
Erfahren Sie, wie unser Bericht Ihr Geschäft optimieren kann, Sprechen Sie mit einem Analysten
Reagenzien & Kits Segment, um die höchste Wachstumsrate aufgrund der Einführung neuer technologisch fortschrittlicher Produkte zu registrieren
Auf der Grundlage des Produkts wird der Markt in Instrumente und Reagenzien und Kits eingeteilt. Das Instrumentesegment hatte 2021 einen dominanten Marktanteil von Covid-19-Diagnostik. Fortgeschrittene Assays und Kits, die von den wichtigsten Akteuren gestartet wurden, um die Nachfrage zu erfüllen, wird die Einnahmen des Segments erhöhen. Zum Beispiel kündigte F. Hoffmann-La Roche Ltd im Dezember 2021 den SARS-COV-2 & Grippe A/B-Antigen-Testplan an. Der Test wird verwendet, um zwischen Covid-19 und Influenza zu unterscheiden.
Andererseits ist der Anteil des Instrumentesegments niedriger, da die meisten vorhandenen diagnostischen Geräte mit den neu entwickelten CoVID-19-Test-Tests kompatibel sind. Das Instrumentesegment wird voraussichtlich mit einem erheblich niedrigen CAGR wachsen.
Durch Technologieanalyse
Höhere Rate der genauen Ausgabe durch PCR -Technik, um die Akzeptanz zu erhöhen
Durch Technologie wird der Markt in eingeteilt inPolymerasekettenreaktion (PCR), Enzymgebundener Immunosorbent-Assay (ELISA), lateraler Flussimunoassay (LFIA) und andere. Das PCR -Techniksegment dominierte den Markt im Jahr 2021. Die Dominanz ist auf die erhöhte Quantifizierung von Patientenproben durch die Verwendung von PCR zurückzuführen. Laut einem von The Hindu im Juni 2020 veröffentlichten Nachrichtenartikel sagten Forscher des Zentrums für Zell- und Molekularbiologie (CCMB), dass die PCR -Methode weniger teuer ist als andere. Daher werden Patientenproben unter Verwendung von PCR weitgehend quantifiziert. Die Einführung neuer PCR-basierter Erkennungstechniken dürfte in den kommenden Jahren die Nachfrage nach PCR-Instrumenten steigen.
Das ELISA-Segment wächst auf einer erheblichen CAGR aufgrund wachsender Genehmigungen für ELISA-basierte Tests durch die US-amerikanische FDA und andere Regulierungsbehörden. Es wird erwartet, dass das LFIA-Segment die zweitführende Position auf dem Markt innehatte. Solche Tests identifizieren die Existenz der neuartigen Coronavirus -Antigene durch nasale oder nasopharyngeale Proben und liefern innerhalb von 15 Minuten Ergebnisse.
Nach Analyse der Probentyp
Oropharyngeal- und Nasopharyngeal -Tupfersegment, die durch steigende Anzahl von Tests angetrieben werden sollen
Nach Probenentyp ist der Markt in oropharyngeale und nasopharyngeale Tupfer, Nasenabstriche und Blut unterteilt. Das oropharyngeale &Nasopharyngeale TupferSegment markierte die höhere Position auf dem Markt aufgrund der erhöhten Covid-19-Tests durch solche Tupfertests. Tupfertests sind einfach, bequem und können schnell durchgeführt werden. Aufgrund des erhöhten Drucks bei der Prüfung von Patienten mit Coronavirus-Infektionen sind diese Tupfertests verbraucherfreundlich und können innerhalb weniger Stunden Ergebnisse liefern. Im Juni 2020 berichtete Global Times, dass Peking 2,29 Millionen Menschen unter Verwendung von Tupfertests zum Screening von CoVID-19-Fällen zwischen 11 untersuchtethUnd 20. JunithJuni.
Das Segment Nasal-Tupfer-Segment hält die zweitführende Position auf dem Markt aufgrund einer höheren Sammlung von Proben für diagnostische Zwecke. Das Blutprobensegment registriert während des prognostizierten Zeitraums eine signifikante CAGR. Forscher haben Blutproben von Patienten gesammelt, um erschöpfende Forschungsaktivitäten durchzuführen, um neuartige Therapien wie Plasma -Therapie zur Behandlung zu bringen.
Durch Festlegen der Analyse
Laborbasiertes Segment, um aufgrund der strengen COVID-19-Diagnose in Labors Traktion zu gewinnen
Durch die Festlegung ist der Markt in Laborbasiert und in Pflegepunkte unterteilt. Das laborbasierte Segment dominierte den Markt im Jahr 2021, da die wachsende Anzahl von Labors mit Hochdurchsatztechnologien anbietet, um CoVID-19-Tests effektiv zu beschleunigen. Zum Beispiel kündigte Hyderabad im Juni 2020 das Indian Institute of Technology die Entwicklung eines Covid-19-Tests für künstliche Intelligenz an, der zu erschwinglichen Kosten durchgeführt werden kann.
Es wird geschätzt, dass das Segment Point of Care (POC) während des prognostizierten Zeitrahmens gemäß dem zweiten Szenario die höchste CAGR aufweist. Das Wachstum ist auf die steigende Anzahl von COVID-19-POC-Tests zurückzuführen, verbunden mit der steigenden Rate der US-amerikanischen FDA-Zulassungen für effiziente und hochempfindliche POC-Tests für die Krankheit. Zum Beispiel erhielt BD im Juli 2020 die Notfallverwaltung (EUA) von der US-amerikanischen Food and Drug Administration (FDA) für sein Veritor-System für die schnelle Erkennung von SARS-COV-2. Dies kann in POC -Einstellungen verwendet werden. Gemäß dem ersten Szenario wird jedoch erwartet, dass das Segment einen Rückgang seines Wachstums aufgrund des abnehmenden Wachstums der Anzahl der COVID-19-Fälle beobachtet.
Durch Endbenutzeranalyse
Zunehmende Anzahl diagnostischer Verfahren zum Antrieb der Laboratorien und diagnostischen Segments
Der Marktanteil ist in Krankenhäusern und Kliniken, Labors und diagnostischen Zentren, Heimtests und andere in Bezug auf Endbenutzer unterteilt. Das Segment Laboratories & Diagnostic Centers wird voraussichtlich im Prognosezeitraum einen dominanten Marktanteil haben. Die Dominanz dieses Segments ist auf die zunehmenden diagnostischen Verfahren und den Verkauf von diagnostischen Produkten in entwickelten und aufstrebenden Volkswirtschaften zurückzuführen.
Das Segment des Hospitals & Clinics Centers wird voraussichtlich bis zum Ende des Prognosezeitraums auf dem globalen Markt für Diagnostik den zweitgrößten Anteil erwerben, da die Patienten mit Patienten mit Covid-19 nach dem ersten Szenario plötzlich steigen. Während im zweiten Szenario der Markt für Heimtests aufgrund der zunehmenden Nachfrage nach schnellen Testkits aufgrund des daraus resultierenden Ausbruchs neuer Covid-19-Varianten voraussichtlich dominieren wird.
Regionale Erkenntnisse
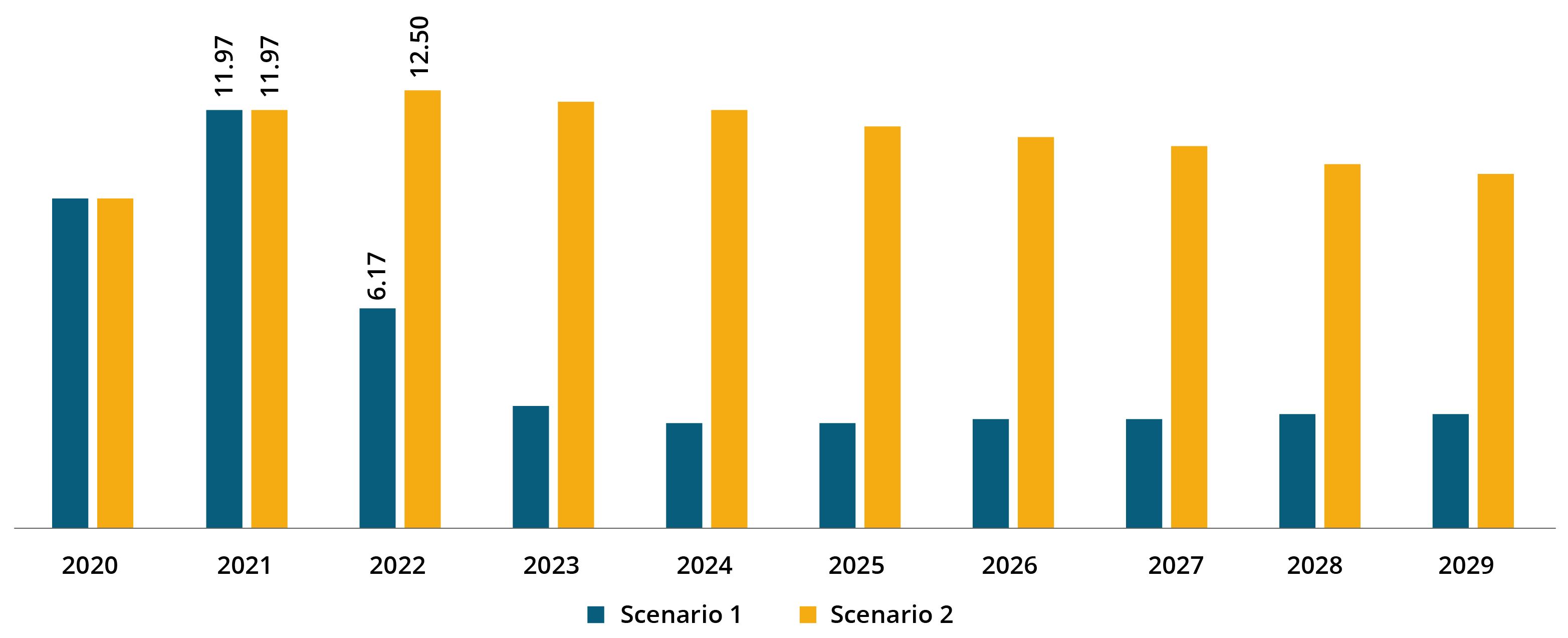
North America COVID-19 Diagnostics Market Size, 2021 (USD Billion)
Um weitere Informationen zur regionalen Analyse dieses Marktes zu erhalten, Laden Sie ein kostenloses Beispiel herunter
Europa dominierte den globalen Markt im Jahr 2021. Die Dominanz dieser Region ist auf die massive Belastung durch Covid-19-Fälle in den meisten europäischen Ländern zurückzuführen und den Schwerpunkt auf mehr Tests für die Kontrolle der Infektionen erhöht. Zum Beispiel wurden nach Angaben der Weltgesundheitsorganisation (WHO) ab dem 8. Januar 2022 15,2 Millionen Fälle in Frankreich registriert. Neue Produkteinführungen in der Region Europas haben auch das Wachstum des Marktes vorantrieben. Zum Beispiel gab die Fujifilm Holdings Corporation im März 2021 bekannt, dass sie ein schnelles Antigen-Testkit für SARS-COV-2 mit Zulassung von CE-Marke in Europa auf den Markt gebracht haben.
Der Markt in Nordamerika lag im Jahr 2021 bei 11,97 Milliarden USD. Gemäß Szenario 2 wird der Markt in der Region voraussichtlich in einer erheblichen CAGR wachsen, da die Zahl der COVID-19-Fälle plötzlich steigt und die Nachfrage nach Diagnostik steigt.
Der Nahe Osten und Afrika werden voraussichtlich im Prognosezeitraum in einem schnellsten CAGR wachsen. Dieses Wachstum ist auf die zunehmende Einführung von Coronavirus -Erkennungskits und Instrumenten zurückzuführen.
Hauptakteure der Branche
Abbott hält aufgrund seines diversifizierten und starken Produktportfolios einen wichtigen Marktanteil
Abbott ist einer der Hauptakteure auf dem Markt. Das Unternehmen vervollständigte 2021 den größten Anteil des Marktes. Der Umsatz von Abbot im Jahr 2021 beobachtete einen Anstieg von 21,8% gegenüber 34,61 Mrd. USD im Jahr 2020. Die Dominanz in diesem Markt ist auf die Ausweitung seines Produktportfolios für die COVID-19-Diagnose zurückzuführen. Neue Produkteinführungen und bedeutende Produktgenehmigungen von Aufsichtsbehörden tragen ebenfalls zu einem hohen Marktanteil bei. Im März 2021 erhielt Abbott die Berechtigung für die Notfallverwendung von der US-amerikanischen Food and Drug Administration (FDA) zur Verwendung von Binaxnow Covid-19 AG-Selbsttest, die zur Erkennung der Infektion verwendet werden kann.
F. Hoffmann-La Roche Ltd ist ein weiterer wichtiger Akteur auf dem globalen Markt. Der Umsatz des Unternehmens für die COVID-19-Diagnostik stieg im Jahr 2021 aufgrund der Einführung mehrerer Produkte. Weitere wichtige Akteure auf dem Markt sind Danaher, Perkinelmer Inc. und Siemens Healthineers AG.
Liste der wichtigsten Unternehmen, die vorgestellt wurden:
- F. Hoffmann-La Roche Ltd (Schweiz)
- Abbott (USA)
- Danaher(UNS.)
- Siemens Healthineers AG(Deutschland)
- Quidel Corporation (USA)
- Biomérieux SA (Frankreich)
- Quest Diagnostics Incorporated (USA)
- Thermo Fisher Scientific Inc. (USA)
- Perkinelmer Inc. (USA)
Schlüsselentwicklungen der Branche:
- Dezember 2021- -Das vertrauenswürdige Labor von DTPM gab bekannt, dass die FDA die Tide Laboratories DTPM COVID-19 RT-PCR-Test-Notwendigkeitsberechtigung neu aufgelegt hat. Bei einer Modifikation erkennt der Test die SARS-CoV-2-Omicron-Variante.
- Oktober 2021 -Perkinelmer Inc. kündigte an, dass die US-amerikanische FDA die Notwendigkeitsbehörde für den PKAMP Respiratory SARS-COV-2 RT-PCR-Panel 1-Assay ausgestellt hat. Dieses RT-PCR-Panel kann verwendet werden, um SARS-CoV-2, Influenza A, Influenza B und Syncytial Virus (RSV) qualitativ nachzuweisen und zu differenzieren.
Berichterstattung
An Infographic Representation of Markt für COVID-19-Diagnostika
Um Informationen zu verschiedenen Segmenten zu erhalten, Teilen Sie uns Ihre Anfragen mit
Der Covid-19-Diagnostik-Marktforschungsbericht bietet eine detaillierte Branchenanalyse. Es konzentriert sich auf wichtige Aspekte wie führende Unternehmen, Produkttyp und Anwendung. Darüber hinaus bietet es Einblicke in die Markttrends und zeigt wichtige Entwicklungen der Branche. Zusätzlich zu den oben genannten Faktoren umfasst der Bericht mehrere Faktoren, die zum Wachstum des Marktes in den letzten Jahren beigetragen haben.
Rahmen und Segmentierung melden
|
ATTRIBUT |
Details |
|
Studienzeitraum |
2020-2029 |
|
Basisjahr |
2021 |
|
Geschätztes Jahr |
2022 |
|
Prognosezeitraum |
2022-2029 |
|
Historische Periode |
2020 |
|
Einheit |
Wert (USD Milliarden) |
|
Segmentierung |
Nach Produkt
|
|
Nach Technologie
|
|
|
Nach Probenentyp
|
|
|
Durch Einstellung
|
|
|
Von Endbenutzer
|
|
|
Durch Geographie
|
Häufig gestellte Fragen
Der globale Marktwert belief sich im Jahr 2021 auf 46,76 Milliarden USD. Fortune Business Insights sagt, dass die globale Marktgröße nach Szenario C bis 2029 auf 8,91 Mio. USD abnimmt. Gemäß Szenario 2 wird die Marktgröße bis 2029 geschätzt.
Der Markt wird voraussichtlich gemäß dem ersten Szenario und einem CAGR von -2,9% gemäß dem zweiten Szenario während des Prognosezeitraums (2022-2029) eine CAGR von -13,1% erleben.
Nach Produkt wird das Segment Reagenzien und Kits den Markt leiten.
Das Wachstum der Anzahl der Covid-19-Tests aufgrund der Anstieg der Anzahl der Fälle wird voraussichtlich das Marktwachstum steigern.
F. Hoffmann-La Roche Ltd, Abbott, Danaher und Perkin Elmer, Inc. sind die Top-Akteure auf dem Markt.
Europa wird voraussichtlich den höchsten Anteil am Markt haben.
Nehmen Sie Kontakt mit unseren Experten auf Sprechen Sie mit einem Experte
Verwandte Berichte
-
US +1 833 909 2966 (Gebührenfrei)
-
Nehmen Sie Kontakt mit uns auf

 View Full Infographic
View Full Infographic

