Autismo: revisión de tuberías, 2024
INFORMACIÓN CLAVE DEL MERCADO
El autismo, ahora también conocido como trastorno del espectro autista, se refiere a un grupo diverso de trastornos del desarrollo neurológico que generalmente se diagnostica durante los años de adolescencia del individuo. El autismo se relaciona particularmente con el desarrollo del cerebro e impacta cómo un individuo interactúa o se comunica en una situación social. La frase del espectro en el "trastorno del espectro autista" refleja la diversa gama de síntomas y su gravedad. Algunos de los trastornos que se encuentran bajo el trastorno del espectro autista incluyen:
- Trastorno autista
- Síndrome de Asperger
- Trastorno de desarrollo generalizado no especificado de otra manera (PDD-NOS)
- Otros
Epidemiología:
Varios estudios recientes han indicado fuertemente que la prevalencia del autismo está aumentando rápidamente, sin embargo, hay una falta de consenso en términos de comprender qué causa estas enfermedades. Por ejemplo, ciertos estudios han indicado que las influencias genéticas y los factores ambientales que incluyen determinantes sociales, como la cobertura limitada del seguro de salud y el estado socioeconómico más bajo pueden causar esta condición. Según los datos publicados por la Organización Mundial de la Salud (OMS) en noviembre de 2023, se estima que 1 de cada 100 niños sufren esta enfermedad a nivel mundial. Además, la OMS continúa reiterando que la prevalencia reportada de esta enfermedad difiere enormemente en varias geografías.
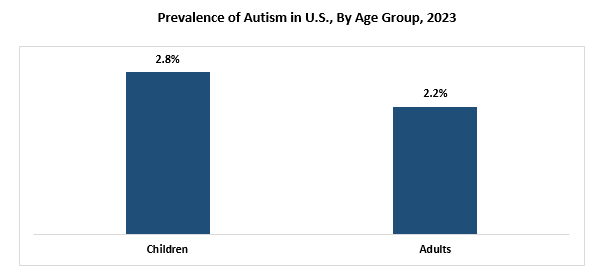
Según los datos publicados por los Centros para el Control y la Prevención de Enfermedades (CDC) en 2023, la prevalencia del autismo ha aumentado en los EE. UU. Actualmente, la prevalencia del autismo en los EE. UU. Es 1 de cada 36 niños, que es considerablemente más alta que la prevalencia previamente reportada de 1 en 44 niños en los EE. UU. Además, el CDC también el CDC también establece que en los EE. UU., 4 en 100 niños y 1 en 100 niñas sufren de esta condición de esta condición.
Evaluación terapéutica:
Diagnóstico:
Según los Centros para el Control y la Prevención de Enfermedades (CDC) de los EE. UU., El diagnóstico de esta afección se basa en dos fuentes de información: la descripción del cuidador de los padres o el cuidado del niño del desarrollo del niño o la evaluación del comportamiento del niño. Los CDC también establecen que el manual de diagnóstico y estadístico de la Asociación Americana de Psiquiatría, Quinta Edición (DSM-5) ofrece un criterio estandarizado para el diagnóstico del trastorno del espectro autista. En términos de los criterios del DSM-5 para el diagnóstico de autismo, el niño debe tener déficits persistentes en cada una de las tres áreas de comunicación e interacción social. De manera similar, en Europa, el diagnóstico del trastorno del espectro autista generalmente implica la participación de un equipo multidisciplinario de psiquiatras, terapeutas del habla y psicólogos. Incluso en Europa, los criterios para el diagnóstico de autismo están estandarizados con la adherencia a las pautas publicadas por el manual de diagnóstico y estadístico de los trastornos mentales (DSM-5) o la clasificación internacional de enfermedades (ICD-11).
Tratamiento:
En términos del tratamiento del autismo, a menudo se considera un enfoque de tratamiento múltiple. Esto incluye la utilización de las terapias de comunicación y comportamiento y las terapias farmacológicas. Varios estudios de investigación han demostrado la fuerte eficacia de la adopción de terapias combinadas para el autismo. Algunas de las terapias de comunicación y comportamiento utilizadas para el trastorno del espectro autista incluyen la terapia del habla y el lenguaje, el análisis del comportamiento aplicado (ABA), la terapia ocupacional, la terapia cognitiva conductual (TCC) y otros. En términos de terapias farmacológicas, a partir de ahora, no se ha aprobado ningún medicamento para tratar o curar el autismo. Sin embargo, ciertos medicamentos se utilizan para ayudar a los profesionales de la salud a controlar los síntomas de esta afección, como irritabilidad, insomnio, depresión y falta de enfoque. Algunas de estas terapias farmacológicas mencionadas han recibido aprobaciones regulatorias de agencias de la FDA de los EE. UU., Mientras que las otras se usan fuera de etiqueta.
Productos clave:
Los medicamentos que han recibido la aprobación de la FDA de EE. UU. Para el tratamiento del trastorno del espectro autista son risperidona y aripiprazol. Si bien se puede recetar risperidona para niños entre las edades de 5 a 16 años para ayudar con la agresión y la irritabilidad, el aripiprazol se puede dar a los niños entre las edades de 6 a 17 años. Sin embargo, en Europa, no hay medicamentos aprobados para el tratamiento de los síntomas del autismo, mientras que ciertas pautas respaldan su utilización.
Los principales jugadores en el autismo:
Algunos de los principales actores en el mercado de autismo son Janssen Global Services, LLC, Amneal Pharmaceuticals LLC, Bristol-Myers Squibb Company, Aurobindo Pharma y otras compañías.
Descripción general del mercado del tratamiento del trastorno del espectro autista:
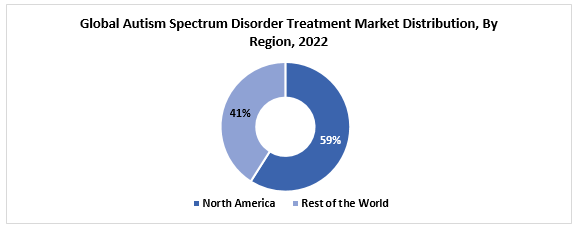
El tamaño del mercado del tratamiento del trastorno del espectro del espectro autista global se valoró en USD 6.94 mil millones en 2022. Se proyecta que el mercado crezca de USD 7.41 mil millones en 2023 a USD 13.14 mil millones para 2030, que exhibe una CAGR de 8.5% durante 2023-2030. La región de América del Norte es la región más dominante en el mercado global. Algunos de los factores que contribuyen al crecimiento del mercado global es la presencia de candidatos potenciales de tuberías que pueden ser aprobados, el fuerte aumento sostenido de la prevalencia del autismo y el impulso en la conciencia entre la población general.
.png)
Análisis de tuberías:
Descripción general de la tubería:
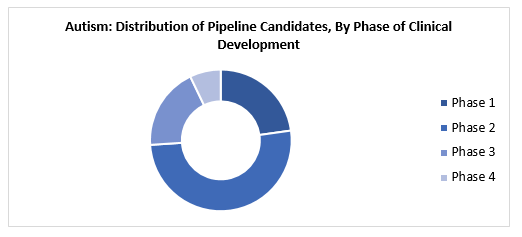
En la actualidad, alrededor del 75% de los candidatos de tuberías para el autismo se encuentran en las etapas de fase 1 y fase 2 de los ensayos clínicos combinados. La mayoría de los estudios están patrocinados por las instituciones de la industria y el gobierno.
Tubería por mecanismo de acción:
El mecanismo de acción de las primeras terapias que han obtenido aprobaciones regulatorias para el autismo como la risperidona y el aripiprazol son el bloqueo de los receptores de serotonina 2a y dopamina D2 para risperidona. Para el aripiprazol, el mecanismo de acción es la estimulación y la inhibición de la dopamina a medida que involucra al receptor D2. En términos de actividad de investigación, varios jugadores se han centrado en los mecanismos genéticos que influyen en el autismo. En los últimos tiempos, algunas de las compañías se han centrado en el siguiente mecanismo de acciones:
- Modulación de catecolaminas:Las catecolaminas son un conjunto de neurotransmisores que se suministra a casi todos los tejidos del cuerpo, y casi todas las extensiones del cerebro, por lo tanto, este es un mecanismo regulador neurológico común para todos los síntomas de autismo. Los medicamentos de la tubería que pertenecen a esta clase de mecanismo de acción pueden liberar un mecanismo presináptico que inhibe la tirosina hidroxilasa y, finalmente, la síntesis, almacenamiento y liberación de todas las catecolaminas. Esto puede regular las catecolaminas al llevarla a un equilibrio homeostático.
- Inhibición de galectina-3:Varios estudios de investigación han señalado que los niveles de proteína galectina-3 son considerablemente más altos en niños con TEA. Por lo tanto, la inhibición de esta proteína puede permitir el control de los síntomas del autismo.
- Digestión de proteínas aceleradas y absorción de aminoácidos:Los medicamentos que pertenecen a este mecanismo de acción, enfatizan el papel de los aminoácidos en los trastornos neurológicos. Esto se debe a que los aminoácidos son un jugador clave en términos de nuevas formaciones de neurotransmisores, la regulación de los genes del SNC y también la síntesis de proteínas. Estas drogas juegan un papel clave en la formación de enzimas que conduce a un grupo de aminoácidos equilibrado. Los estudios relacionados con este candidato de tubería han indicado que las deficiencias enzimáticas juegan un papel en el autismo.
Tubería por ruta de administración:
En términos de la ruta de administración de los medicamentos de la tubería, un número significativo de estos medicamentos en ensayos clínicos para el tratamiento del autismo tiene la ruta oral de administración. Esto se debe a que, como varios pacientes de autismo son adolescentes, la forma oral de la administración de medicamentos será más fácil para ellos y los hará más tratamiento adherente a medida que sus padres o cuidadores puedan administrarlos en los entornos de atención domiciliaria.
Tubería, por tipo de molécula:
La mayoría de los jugadores que participan en los ensayos clínicos para el tratamiento del autismo se han centrado en el desarrollo de los medicamentos de moléculas pequeñas. Algunos de los jugadores con medicamentos de molécula pequeña en sus tuberías de productos para el autismo incluyen la compañía emergente de la terapéutica axial.
Tubería, por empresa:
En términos de fármacos de tuberías para el tratamiento del autismo, el número de estos medicamentos en las etapas avanzadas de los estudios clínicos es limitado. Varias de las compañías con candidatos de tuberías para el tratamiento del autismo son compañías biofarmacéuticas emergentes, con sede en los EE. UU., Algunas de las compañías con medicamentos de tuberías son Yamo Pharmaceuticals, Curemark y Astrogen, Inc.
Insights de ensayo clínico:
Ensayos clínicos en curso:Algunos de los candidatos clave de tuberías en ensayos clínicos son los siguientes:
Fase 1:
- STP1: Stalicla SA
- Descripción del estudio:El objetivo principal de este estudio es evaluar la seguridad y la tolerabilidad, la farmacocinética y la farmacodinámica, así como la eficacia exploratoria del candidato de la tubería de STP1 en un subgrupo de pacientes que padecen el trastorno del espectro autista (TEA).
- SB-121: Scioto Biosciences, Inc.
- Descripción del estudio:Este estudio es un estudio cruzado de dosis múltiples, aleatorizado, doble ciego, controlado con placebo, que evalúa la seguridad y la tolerabilidad de múltiples dosis de SB-121 durante un período de 28 días para un grupo de sujetos en el grupo de edad de 15 a 45 años, diagnosticados con trastorno autista.
Fase 2:
- ML-004: Maplight Therapeutics
- Descripción del estudio:Este modelo de estudio es un estudio múltiple, aleatorizado, doble ciego, de grupo paralelo, controlado con placebo que reclutará aproximadamente 150 adolescentes y sujetos adultos que padecen TEA. El objetivo principal de este ensayo clínico es estudiar la eficacia de este fármaco de la tubería en comparación con el placebo en términos de la mejora de los déficits de comunicación social en pacientes que padecen TEA. El tipo de estudio de este ensayo clínico es intervencionista, siendo el tratamiento el propósito principal. El enmascaramiento en este estudio es cuádruple, con el modelo de intervención como asignación paralela. La asignación para este ensayo clínico es aleatorizado.
- ARD-501: Aardvark Therapeutics, Inc.
- Descripción del estudio:Este estudio es un ensayo cruzado cegado, controlado con placebo, que evalúa la seguridad de los dos niveles de dosis del candidato de la tubería de ARD-501 en pacientes con TEA de TEA. El tipo de estudio del ensayo clínico es intervencionista, y el propósito principal es el tratamiento. La asignación es aleatoria para este estudio, y el modelo de intervención es la asignación de cruce. El enmascaramiento de este estudio es el doble.
Fase 3:
- CM-AT: CureMark
- Descripción del estudio:Este estudio es un estudio de extensión abierta de CM-AT para el tratamiento de niños que padecen autismo con todos los niveles de quimotripsina fecal. CM-AT es una enzima patentada que se administrará a los niños que padecen este trastorno, tres veces al día. El tipo de estudio de este ensayo clínico es intervencionista, y el propósito principal es el tratamiento. El modelo de intervención es una asignación de grupo único y el enmascaramiento es NINGUNO (etiqueta abierta).
- AZD0901: Astrógeno, Inc.
- Descripción del estudio:Este estudio tiene como objetivo demostrar la eficacia y la seguridad de AST-001, en comparación con el placebo, en términos de la mejora de los síntomas centrales del trastorno del espectro autista (TEA) en los niños. Para este estudio, el tipo de estudio es intervencionista y el propósito principal es el tratamiento. La asignación para este ensayo clínico es aleatorizado, y el modelo de intervención es una asignación paralela. El enmascaramiento de este ensayo clínico es cuádruple.
Perspectivas de prueba futuras:
- Enero de 2024:La Compañía Farmacéutica de SPARC con sede en Israel anunció el comienzo del ensayo clínico para comparar los efectos de la terapia Sci-210 con el tratamiento estándar de CBD para el manejo de los síntomas de TEA.
- Noviembre de 2021: Axial Therapeutics anunció la dosificación de los primeros sujetos en el ensayo clínico global de fase 2B para la irritabilidad asociada con el trastorno del espectro autista (TEA).
Paisaje regulatorio:
- Aprobaciones de la FDA y EMA:En términos de agencias reguladoras, la FDA y EMA de EE. UU. Son las agencias clave. Hasta la fecha, la FDA de los Estados Unidos ha otorgado la aprobación a 2 medicamentos para el manejo de los síntomas del autismo, y la EMA no ha otorgado aprobaciones hasta la fecha. Sin embargo, para reducir esta limitación de no aprobaciones hasta la fecha, tiene la formación de consorcios, como el consorcio AIMS-2-Entrals.
- Designaciones de drogas huérfanas:El número de medicamentos que reciben la designación regulatoria de la FDA de los EE. UU. De una designación de fármacos huérfanos (impar) ha sido relativamente limitado. Sin embargo, en febrero de 2023, la FDA de los EE. UU. Otorgó un extraño al medicamento Ketarx (ketamina), que actualmente se encuentra en ensayos clínicos de fase 2 para el tratamiento del síndrome de Rett, que se considera una enfermedad en el espectro autista.
- Desafíos de autorización del mercado:Algunos de los desafíos de autorización del mercado que enfrentan los candidatos a la tubería de autismo incluyen la falta de aprobaciones regulatorias y el escepticismo en términos de su capacidad para tratar los síntomas centrales de la enfermedad.
Alcance de informes
- Una evaluación exhaustiva de los productos de tuberías por áreas como la etapa de desarrollo; ruta de administración; clase de drogas; indicación; patrocinador; Tipo de molécula y objetivo fármaco
- Perfiles completos de los productos de tuberías con detalles como la descripción general de la empresa; Descripción del Producto; Estado de I + D; actividades de desarrollo; mecanismo de acción; tipo de molécula; etapa de desarrollo; indicaciones; financiación y ruta de administración
- Descripción general de los productos de tuberías latentes y descontinuados
- Conocimientos clave sobre la epidemiología de las condiciones que se tratan por los productos de la tubería y la descripción general del mercado direccionable o actual para los productos de la tubería
- Descripción general de los últimos desarrollos; Artículos de noticias, comunicados de prensa y conferencias relevantes
Metodología de informes
- Todos los informes de tuberías se construyen mediante el análisis de datos recopilados principalmente a través de fuentes de investigación de escritorio creíbles. La investigación secundaria se complementa con entrevistas realizadas con líderes de opinión clave.
- Las fuentes de investigación del escritorio incluyen bases de datos de ensayos clínicos globales y regionales; informes anuales, sitios web, comunicados de prensa y presentaciones de inversores de empresas; papeles blancos; artículos de noticias; informes publicados por asociaciones de la industria; artículos/informes publicados en bases de datos como NCBI, Researchgate; bases de datos internas
Razones para comprar este informe
- Desarrollar estrategias de crecimiento efectivas basadas en una descripción completa de la actividad de I + D y los productos de tuberías para el autismo
- Identificar jugadores emergentes o competencia en el mercado basado en productos de tuberías y desarrollar estrategias para contrarrestar la aparición de estos jugadores
- Identificar el enfoque de los principales jugadores sobre I + D para el autismo
- Identificar compañías potenciales desde una asociación o punto de vista de adquisición basado en la sinergia actual en actividades o estrategias de I + D para diversificar el enfoque de I + D para impulsar el crecimiento de los negocios
- Analice las razones detrás de los productos latentes y descontinuados para hacer cambios en el enfoque de I + D si es necesario

