Autisme: Revue du pipeline, 2024
APERÇUS CLÉS DU MARCHÉ
L'autisme, maintenant également appelé trouble du spectre de l'autisme, fait référence à un groupe diversifié de troubles neurodéveloppementaux qui est généralement diagnostiqué pendant les années adolescentes de l'individu. L'autisme se rapporte particulièrement au développement du cerveau et a un impact sur la façon dont un individu interagit ou communique dans une situation sociale. L'expression du spectre dans le «trouble du spectre autistique» reflète la diversité des symptômes et leur gravité. Certains des troubles qui relèvent du trouble du spectre de l'autisme comprennent:
- Trouble autistique
- Syndrome d'Asperger
- Trouble de développement omniprésent non spécifié autrement (PDD-NOS)
- Autres
Épidémiologie:
Plusieurs études récentes ont fortement indiqué que la prévalence de l'autisme augmente rapidement, cependant, il y a un manque de consensus en termes de compréhension de ce qui cause ces maladies. Par exemple, certaines études ont indiqué que les influences génétiques et les facteurs environnementaux qui comprennent des déterminants sociaux tels que la couverture d'assurance des soins de santé limitée et un statut socioéconomique inférieur peuvent provoquer cette condition. Selon les données publiées par l'Organisation mondiale de la santé (OMS) en novembre 2023, environ 1 enfant sur 100 souffre de cette maladie dans le monde. De plus, l'OMS continue en réitérant que la prévalence signalée de cette maladie diffère considérablement entre diverses géographies.
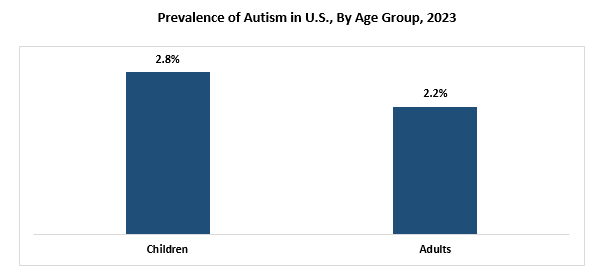
Selon les données publiées par Centers for Disease Control and Prevention (CDC) en 2023, la prévalence de l'autisme a augmenté aux États-Unis actuellement, la prévalence de l'autisme aux États-Unis est de 1 enfant sur 36, ce qui est considérablement plus élevé que la prévalence précédemment signalée de 1 garçons sur 44 aux États-Unis en outre, le CDC indique également que aux États-Unis, 4 sur 100 garçons et 1 chez 100 personnes souffrent de cette condition.
Évaluation thérapeutique:
Diagnostic:
Selon les Centers for Disease Control and Prevention (CDC) des États-Unis, le diagnostic de cette condition repose sur deux sources d’information: la description par les parents ou la soignante de l’enfant du développement de l’enfant ou l’évaluation professionnelle du comportement de l’enfant. Le CDC indique également que le manuel diagnostique et statistique de l'American Psychiatric Association, la cinquième édition (DSM-5) donne un critère standardisé pour le diagnostic du trouble du spectre autistique. En termes de critères du DSM-5 pour le diagnostic de l'autisme, l'enfant doit avoir des déficits persistants dans chacun des trois domaines de la communication et de l'interaction sociales. De même en Europe, le diagnostic du trouble du spectre autistique implique généralement l'implication d'une équipe multidisciplinaire de psychiatres, d'orthophonistes et de psychologues. Même en Europe, les critères de diagnostic de l'autisme sont normalisés avec l'adhésion aux directives publiées par le manuel diagnostique et statistique des troubles mentaux (DSM-5) ou la classification internationale des maladies (CIM-11).
Traitement:
En termes de traitement de l'autisme, une approche de traitement à plusieurs volets est souvent prise en compte. Cela comprend l'utilisation des thérapies de communication et de comportement et les thérapies médicamenteuses. Plusieurs études de recherche ont démontré la forte efficacité de l'adoption de thérapies combinées pour l'autisme. Certaines des thérapies de communication et comportementaux utilisées pour le trouble du spectre autistique comprennent la parole et le langage, l'analyse comportementale appliquée (ABA), l'ergothérapie, la thérapie cognitivo-comportementale (TCC) et d'autres. En termes de thérapies médicamenteuses, à ce jour, aucun médicament n'a été approuvé pour traiter ou guérir l'autisme. Cependant, certains médicaments sont utilisés pour aider les professionnels de la santé à gérer les symptômes de cette condition tels que l'irritabilité, l'insomnie, la dépression et le manque de concentration. Certaines de ces thérapies médicamenteuses mentionnées ont reçu des approbations réglementaires des agences de la FDA américaine, tandis que les autres sont utilisés hors AMM.
Produits clés:
Les médicaments qui ont reçu l'approbation de la FDA américaine pour le traitement du trouble du spectre autistique sont la rispéridone et l'aripiprazole. Alors que la rispéridone peut être prescrite pour les enfants âgés de 5 à 16 ans pour aider à l'agression et à l'irritabilité, l'aripiprazole peut être donné aux enfants âgés de 6 à 17 ans. Cependant, en Europe, il n'y a pas de médicaments approuvés pour le traitement des symptômes de l'autisme, tandis que certaines directives soutiennent leur utilisation.
Acteurs majeurs de l'autisme:
Certains des principaux acteurs du marché de l'autisme sont Janssen Global Services, LLC, Amneal Pharmaceuticals LLC, Bristol-Myers Squibb Company, Aurobindo Pharma et d'autres sociétés.
Présentation du marché du traitement des troubles du spectre autistique:
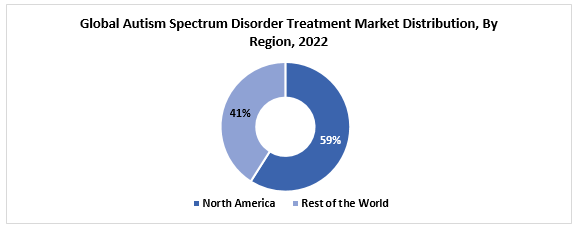
La taille du marché mondial du traitement des troubles du spectre autistique était évaluée à 6,94 milliards USD en 2022. Le marché devrait passer de 7,41 milliards USD en 2023 à 13,14 milliards USD d'ici 2030, présentant un TCAC de 8,5% en 2023-2030. La région de l'Amérique du Nord est la région la plus dominante du marché mondial. Certains des facteurs qui contribuent à la croissance du marché mondial sont la présence de candidats potentiels des pipelines qui peuvent être approuvés, la forte augmentation soutenue de la prévalence de l'autisme et la stimulation de la sensibilisation de la population générale.
.png)
Analyse du pipeline:
Aperçu du pipeline:
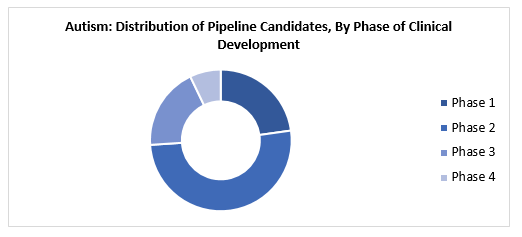
À l'heure actuelle, environ 75% des candidats au pipeline pour l'autisme sont dans les stades de phase 1 et de phase 2 des essais cliniques combinés. La majorité des études sont parrainées par des institutions industrielles et gouvernementales.
Pipeline par mécanisme d'action:
Le mécanisme d'action des premières thérapies qui ont obtenu des approbations réglementaires pour l'autisme tels que la rispéridone et l'aripiprazole sont le blocage de la sérotonine 2A et des récepteurs D2 dopamine D2 pour la rispéridone. Pour l'aripiprazole, le mécanisme d'action est la stimulation et l'inhibition de la dopamine car elle engage le récepteur D2. En termes d'activité de recherche, plusieurs acteurs se sont concentrés sur les mécanismes génétiques influençant l'autisme. Ces derniers temps, certaines des entreprises se sont concentrées sur le mécanisme des actions suivant:
- Modulation des catécholamines:Les catécholamines sont un ensemble de neurotransmetteurs qui est fourni à presque tous les tissus du corps, et presque tous les tracts du cerveau, il s'agit donc d'un mécanisme de régulation neurologique commun pour tous les symptômes de l'autisme. Les médicaments de pipeline appartenant à cette classe de mécanisme d'action peuvent libérer un mécanisme présynaptique qui inhibe la tyrosine hydroxylase, et éventuellement la synthèse, le stockage et la libération de toutes les catécholamines. Cela peut réguler les catécholamines en le ramenant à un équilibre homéostatique.
- Inhibition de la galectine-3:Plusieurs études de recherche ont noté que les niveaux de protéine galectine-3 sont considérablement plus élevés chez les enfants atteints de TSA. Par conséquent, l'inhibition de cette protéine peut permettre le contrôle des symptômes de l'autisme.
- Digestion accélérée des protéines et absorption des acides aminés:Les médicaments appartenant à ce mécanisme d'action mettent l'accent sur le rôle des acides aminés dans les troubles neurologiques. En effet, les acides aminés sont un acteur clé en termes de nouvelles formations de neurotransmetteurs, de régulation des gènes du SNC, ainsi que de la synthèse des protéines. Ces médicaments jouent un rôle clé dans la formation d'enzymes qui conduit à un pool d'acides aminés équilibrés. Les études liées à ce candidat de pipeline ont indiqué que les carences enzymatiques jouent un rôle dans l'autisme.
Pipeline par voie d'administration:
En termes de voie d'administration des médicaments sur le pipeline, un nombre important de ces médicaments sous essais cliniques pour le traitement de l'autisme ont la voie orale d'administration. En effet, comme un certain nombre de patients d'autisme sont des adolescents, la forme orale de l'administration de médicaments sera plus facile pour eux et les rendra plus adhérents au traitement car ils peuvent être administrés par leurs parents ou soignants en milieu à domicile.
Pipeline, par type de molécule:
La majorité des acteurs engagés dans les essais cliniques pour le traitement de l'autisme se sont concentrés sur le développement des médicaments à petites molécules. Certains des joueurs avec des médicaments à petites molécules dans leurs pipelines de produit pour l'autisme comprennent la société émergente de la thérapeutique axiale.
Pipeline, par entreprise:
En termes de médicaments par pipeline pour le traitement de l'autisme, le nombre de ces médicaments aux stades avancés des études cliniques est limité. Un certain nombre de sociétés ayant des candidats au pipeline pour un traitement autistique sont émergentes des sociétés biopharmaceutiques qui basées aux États-Unis, certaines des sociétés ayant des médicaments sur les pipelines sont Yamo Pharmaceuticals, Curemark et Astrogène, Inc.
Informations sur les essais cliniques:
Essais cliniques en cours:Certains des candidats clés du pipeline dans les essais cliniques sont les suivants:
Phase 1:
- STP1: Stalicla SA
- Description de l'étude:L'objectif principal de cette étude est d'évaluer la sécurité et la tolérabilité, la pharmacocinétique et la pharmacodynamique, ainsi que l'efficacité exploratoire du candidat du pipeline de STP1 dans un sous-groupe de patients souffrant d'un trouble du spectre autistique (TSA).
- SB-121: Scioto Biosciences, Inc.
- Description de l'étude:Cette étude est une étude croisée multi-dose, randomisée, en double aveugle et contrôlée par placebo, évaluant la sécurité et la tolérabilité de plusieurs doses de SB-121 sur une période de 28 jours pour un groupe de sujets dans le groupe d'âge de 15 à 45 ans, diagnostiqué avec un trouble autiste.
Phase 2:
- ML-004: Maplight Therapeutics
- Description de l'étude:Ce modèle d'étude est une étude multicentrique, randomisée, en double aveugle et à groupe parallèle, contrôlé par placebo qui recrutera environ 150 adolescents et sujets adultes souffrant de TSA. L'objectif principal de cet essai clinique est d'étudier l'efficacité de ce médicament de pipeline par rapport au placebo en termes d'amélioration des déficits de communication sociale chez les patients souffrant de TSA. Le type d'étude de cet essai clinique est interventionnel, le traitement étant l'objectif principal. Le masquage dans cette étude est quadruple, le modèle interventionnel étant une affectation parallèle. L'allocation de cet essai clinique est randomisée.
- ARD-501: Aardvark Therapeutics, Inc.
- Description de l'étude:Cette étude est un essai croisé en aveugle contrôlé par placebo qui évalue la sécurité des deux niveaux de dose du candidat du pipeline de l'ARD-501 chez les patients souffrant de TSA. Le type d'étude de l'essai clinique est interventionnel et l'objectif principal est le traitement. L'allocation est randomisée pour cette étude et le modèle interventionnel est une affectation croisée. Le masquage de cette étude est double.
Phase 3:
- CM-AT: Curemark
- Description de l'étude:Cette étude est une étude d'extension ouverte de CM-AT pour le traitement des enfants souffrant d'autisme avec tous les niveaux de chymotrypsine fécale. CM-AT est une enzyme propriétaire qui sera administrée aux enfants souffrant de ce trouble, trois fois par jour. Le type d'étude de cet essai clinique est interventionnel, l'objectif principal étant le traitement. Le modèle interventionnel est une affectation de groupe unique et le masquage n'est pas (Labé ouvert).
- AZD0901: Astrogène, Inc.
- Description de l'étude:Cette étude vise à démontrer l'efficacité et l'innocuité de l'AST-001, par rapport au placebo, en termes d'amélioration des symptômes de base du trouble du spectre autistique (TSA) chez les enfants. Pour cette étude, le type d'étude est interventionnel et l'objectif principal est le traitement. L'allocation de cet essai clinique est randomisée et le modèle interventionnel est une affectation parallèle. Le masquage de cet essai clinique est quadruple.
Perspectives futures de procès:
- Janvier 2024:La société pharmaceutique basée en Israël de SCI SPARC a annoncé le début des essais cliniques pour comparer les effets de la thérapie SCI-210 avec le traitement standard du CBD pour la gestion des symptômes de TSA.
- Novembre 2021: Axial Therapeutics a annoncé le dosage des premiers sujets de l'essai clinique mondial de la phase 2B pour l'irritabilité associée au trouble du spectre autistique (TSA).
Paysage réglementaire:
- Approbations de la FDA et de l'EMA:En termes d'organismes de réglementation, la FDA américaine et l'EMA sont les principales agences. Jusqu'à ce jour, la FDA américaine a accordé l'approbation à 2 médicaments pour la gestion des symptômes de l'autisme, et l'EMA n'a accordé aucune approbation jusqu'à ce jour. Cependant, pour réduire cette limitation de non-approbations jusqu'à ce jour, il y a la formation de consortiums tels que le consortium AIMS-2-Trials.
- Des désignations de médicaments orphelins:Le nombre de médicaments recevant la désignation réglementaire de la FDA américaine d'une désignation de médicaments orphelins (impair) a été relativement limité. Cependant, en février 2023, la FDA américaine a accordé un impair au médicament Ketarx (kétamine), qui est actuellement dans les essais cliniques de phase 2 pour le traitement du syndrome de Rett, qui est considéré comme une maladie sur le spectre de l'autisme.
- Défis d'autorisation du marché:Certains des défis d'autorisation du marché auxquels sont confrontés les candidats au pipeline de l'autisme comprennent un manque d'approbation réglementaire et le scepticisme en termes de capacité à traiter les principaux symptômes de la maladie.
Portée
- Une évaluation approfondie des produits du pipeline par des domaines tels que le stade de développement; voie d'administration; classe de drogue; indication; parrainer; Type de molécule et cible médicament
- Profils complets des produits du pipeline avec des détails tels que l'aperçu de l'entreprise; Description du produit; Statut de R&D; activités de développement; mécanisme d'action; type de molécule; étape de développement; indications; financement et voie d'administration
- Aperçu des produits de pipeline dormants et abandonnés
- Des informations clés sur l'épidémiologie des conditions traitées par les produits du pipeline et l'aperçu du marché adressable ou actuel pour les produits du pipeline
- Aperçu des derniers développements; Articles de presse, communiqués de presse et conférences pertinentes
Méthodologie de rapport
- Tous les rapports de pipeline sont construits grâce à l'analyse des données principalement collectées par le biais de sources de recherche de bureau crédibles. La recherche secondaire est complétée par des entretiens menés par des leaders d'opinion clés.
- Les sources de recherche de bureau comprennent les bases de données mondiales et régionales des essais cliniques; Rapports annuels, sites Web, communiqués de presse et présentations d'investisseurs des entreprises; Livre blancs; articles de presse; rapports publiés par les associations de l'industrie; Articles / rapports publiés sur des bases de données telles que NCBI, ResearchGate; bases de données internes
Raisons d'acheter ce rapport
- Développer des stratégies de croissance efficaces basées sur un aperçu complet de l'activité de la R&D et des produits de pipeline pour l'autisme
- Identifier les acteurs émergents ou la concurrence sur le marché en fonction des produits de pipeline et élaborez des stratégies pour contrer l'émergence de ces acteurs
- Identifiez l'objectif des principaux acteurs sur la R&D pour l'autisme
- Identifiez les entreprises potentielles à partir d'un partenariat ou d'un point de vue d'acquisition en fonction de la synergie actuelle dans les activités de R&D ou des stratégies pour diversifier l'objectif de la R&D pour stimuler la croissance de l'entreprise
- Analysez les raisons des produits dormants et abandonnés pour apporter des modifications à la concentration de R&D si nécessaire

